Som forrige blogginnlegg med tittelen antyder «Med fokus på ME-syke barn og unge: De livsviktige patofysiologiske avviksfunnene dr. Helland ALDRI snakker høyt om«, fortsettes vi å se og formidle:
at Der eksisterer sterk evidens på at der er en sentral dysregulering av neuro-endokrine reguleringsmekanismer og funksjon hos ME-syke barn og unge i Norge.

«Forskning med fokus på autonom sirkulasjons- og temperaturregulering hos ungdommer med CFS/ME. Pasientgruppen rapporterte symptomer forenlig med forstyrrelser i disse reguleringsmekanismene, og hadde også signifikant høyere hjertefrekvens, blodtrykk, total perifer motstand, sentral kroppstemperatur og plasmakonsentrasjon av katekolaminer i hvile sammenliknet med en frisk kontrollgruppe. Ortostatisk belastning medførte en kraftigere økning av hjertefrekvens, blodtrykk og total perifer motstand hos pasientene, mens lokal nedkjøling ga et kraftigere fall. I kroppstemperatur og en mindre reduksjon i fingerhuden blodstrøm. I sum indikerer disse resultatene at pasienter med kronisk utmattelsessyndrom har økt sympatisk nerveaktivitet i hvile og avvikende sympatisk respons på beskjedne fysiologiske belastninger.
Karakteren i responsene peker mot en forstyrrelse i sentralnervesystemets kontroll av homeostatiske reguleringsmekanismer. Det finnes holdepunkter for at en slik forstyrrelse ikke bare bør betraktes som et fenomen på linje med mange andre, men at den kan ha sentral patofysiologisk betydning. (VB Wyller, 2009)»
Rikshospitalets forskning på ME syke barn og unge har vedvart siden 2003.
Her er en liten oversikt:
Wyller phd-studie: hhv 27 pasienter/33 HC og 15 pasienter/57 HC
I løpet av prosjektperioden fra august 2007 til april 2009, barn og ungdom CFS pasienter mellom 12 – 18 år ble rekruttert for prosjekt «an observational prospective study on the clinical course of adolescent CFS»
47 pasienter ble inkludert, mens bare 38 pasienter (8 gutter, 30 jenter) fullførte studieprotokollen og gjenstand for analyse. Friske kontroller fra phd-prosjekt 57 HC.
NorCapital: ble søkt REK Sør-Øst 6 mai 2009 og godkjent 1 juni 2009 Inklusjon startet 1 mars 2010. 120 pasienter og 68 HC, ferdigstillt.
PI-EBV studie: Inklusjon start 1. mars 2015, 200 inkluderte pasienter (12 -20 år) og 70 HC ble nådd i desember 2016. Ferdigstillt: juni 2017
Ja, akkurat! Ikke rent lite systematisk forskning på hva ME og utmattelse innebærer…. mange pasienter…mange friske mennesker for sammenligning og sålang vet vi jo ikke hvor mange som kommer til å få ME av kyssesykeviruset..
Der er kanskje ikke så enkelt å «bare hvile» når du rammes av ME, eller «skjerpe seg», eller å bli fortalt at «der feiler deg intet». Du er bare perfeksjonistisk og har blitt ramma av latskap og dårskap. Forskninga på barn og ungdom viser faktisk noe helt annet… Vi skal se på resultatene og funnene i fra publikasjon; Sommerfeldt L, Portilla H, Jacobsen L, Gjerstad J, Wyller VB. Polymorphisms of adrenergic cardiovascular control genes are associated with adolescent chronic fatigue syndrome. Acta Paediatr. 2011 og kort om publikasjonen i fra NorCapital-studien; Hall, Kathryn T. et al.(2016) “Genetic Variation in Catechol-O-Methyltransferase Modifies Effects of Clonidine Treatment in Chronic Fatigue Syndrome.” The pharmacogenomics journal. I tillegg til litt her og der i fra.
Katekol-O-metyltransferase (COMT) eng; catechol-O-methyl transferase, er ett av flere enzymer i kroppen som er involvert i nedbrytningen av katekolaminer som dopamin, noradrenalin og adrenalin. Enzymet overfører en metylgruppe til signalsubstansen fra donatorgruppen SAM (S-adenosylmetionin). Det eksisterer ulike polymorfe genvarianter for COMT-genet.
Altså DNA fra 53 pasienter med CFS, mellom 12-18 år, ble analysert for fem single nucleotide polymorphisms (SNPs). For genotyper (polymorfe genvarianter) av enzymet Katekol-O-metyltransferase (COMT SNP Rs4680), for β₂ -adrenerg reseptor (to SNPs hhv Rs1042714 og Rs1042713), for β₁ – adrenerg reseptor (SNP Rs1801253 og for α₂(a) -adrenerg reseptor (SNP Rs1800544).
…og der starter tilstand sympatikus, aktivitetsrus, må hvile-hvile-hvile, må spare-spare-spare, ka i H**lvte???
Line Sommerfeldt er førsteforfatter på denne studien og dette sier så denne:
[mhjkom: oversettelse etter beste evne]
Introduksjon
Det kroniske utmattelsessyndrom (CFS) er en vanlig og invalidiserende sykdom, karakterisert ved alvorlig utmattelse og tilhørende symptomer som smerte i muskel-og skjelettet system, ikke tilfriskende søvn, sår hals, ømme lymfeknuter, konsentrasjonsproblemer og hodepine (1). Den underforliggende sykdomsmekanismen er stort sett ukjent. Tidligere har vi rapportert forhøyede nivåer av adrenalin (Epinefrin) og noradrenalin (norepinefrin) under hvile blant unge CFS-pasienter sammenlignet med friske kontroller (2). Også, sammenlignet med kontroller, hadde CFS-pasienter høyere blodtrykk, hjertefrekvens og total perifer motstand og LF/HF ratio (en indeks for sinus node sympathicovagal balanse, avledet fra spektralanalyse av hjertefrekvensen) ved hvile, og en kraftigere økning i disse variablene ved ortostatisk stress (3, 4, 5). Andre studier foreslår også en sammenheng mellom katekolamin-nivåer og CFS-symptomer som utmattelse og smerteoverfølsomhet (6,7). Til sammen, disse studiene indikerer en forsterket aktivitet i det sympatiske nervesystemet i CFS, som muligens bidrar til underforliggende patofysiologi (8).
Tvilling studier indikerer en moderat arvelighet av CFS (9), og molekylære analyser foreslår en tilknytning til polymorfismer i gener involvert i metabolisme og funksjon av katekolaminer (10). Interessant, lignende assosiasjoner har blitt dokumentert i lidelser med flere kliniske markører som er felles med CFS, som Postural ortostatisk Takykardi syndrom (POTS), fibromyalgi og kroniske smertesyndromer (11, 12, 13, 14).
Videre er genetiske polymorfismer kjent for å påvirke kardiovaskulære variabler. For eksempel, polymorfismer i β₂- reseptoren er assosiert med individuelle variasjoner i hjerterytme, blodtrykk, hjerteutgang og vasodilatasjon, både i dynamisk og i hvilestatus (11, 15, 16, 17), mens visse polymorfier av β₁- reseptoren er relatert til vasovagal synkope (18).
Målet med denne studien er å kartlegge for en mulig sammenheng mellom polymorfismer av adrenerge kardiovaskulære kontrollgener og barne- og ungdoms CFS.
Vi arbeidet utifra en hypotese om at polymorfe frekvenser av gener som koder for adrenerge reseptor proteiner α₂(a), β₁ og β₂, og det katabolske enzymet katechol-0-metyltransferase (COMT) ville være forskjellig blant CFS ungdom sammenlignet med en referansepopulasjon.
Videre ønsket vi å se om der er en sammenheng mellom disse polymorfiene og variabler som indikerer endret sympatisk kardiovaskulær kontroll i gruppen av CFS-pasienter.
Altså DNA fra 53 pasienter med CFS, mellom 12-18 år, ble analysert for fem single nucleotide polymorphisms (SNPs). For genotyper (polymorfe genvarianter) av enzymet Katekol-O-metyltransferase (COMT SNP Rs4680), for β₂ -adrenerg reseptor (to SNPs hhv Rs1042714 og Rs1042713), for β₁ – adrenerg reseptor (SNP Rs1801253 og for α₂(a) -adrenerg reseptor (SNP Rs1800544). Frekvensen av de polymorfe variantene ble sammenlignet med en referansepopulasjon/gruppe hentet i fra databasen fra «the National Center for Biotechnology Information (NCBI)», vurdering om det foreligger en samvariasjon mellom bestemte genetiske varianter og objektive utfallmål av autonom kardiovaskulær respons på en 20° head-up tilt-test.
SNP: Single (or Simple) nucleotide polymorphism
Aktuell hjertefrekvens, arterielt blodtrykk og slagvolum ble oppnådd fra henholdsvis EKG, høyrefinger-fotoplethysmografi og thoraximpedans; Sistnevnte er ikke rapportert i denne artikkelen.
RR-intervallet (RRI) fra hjertefrekvensopptaket ble satt for spektralanalyse ved hjelp av en adaptiv autoregressiv algoritme som skaper et tidsvarierende spektrum. Spektral kraftdensiteter (absolutte verdier) ble beregnet i lavfrekvent (LF) båndet (0,04-0,15 Hz) og høyfrekvente (HF) båndet (0,15-0,4 Hz); Vi har også beregnet LF/HF-forholdet. Disse indeksene er uttrykk for autonom pulskontroll: HF-variabiliteten til RRI betraktes som en indeks for vagal (parasympatisk) modulering av hjertefrekvens, mens LF-variabiliteten til RRI skyldes den kombinerte effekten av hjertevagal og sympatisk aktivitet; LF/HF-forholdet er et mål for «sympathovagal balanse». (balansen mellom parasympatisk og sympatisk nervesystem PNS balanse)
Resultater
53 pasienter med CFS ble inkludert i studien, 40 % menn, 11-18 år (tabell 1) med kardiovaskulære egenskaper som beskrevet i tabell 2. Signifikante forskjeller i genotype frekvens mellom CFS-pasienter og referansesettet ble funnet for COMT SNP ved Rs 4680 og β₂-reseptor SNP ved rs 1042714 (tabell 3).


For COMT SNP på Rs4680; Frekvensen av AA-genotypen (Met/Met) var høyere og frekvensen av G inneholdende genotyper AG (Met/Val) og GG (Val/Val) var lavere blant CFS-pasienter (p = 0,046).
For den β₂- adrenerge reseptor SNP rs1042714 hadde CFS-pasientene høyere frekvens av den heterozygote genotypen (CG) og lavere frekvens av den homozygot genotypen sammenlignet med referansesettet (p = 0,003). På samme locus, GG genotypen dukket opp med en lavere, mens C -holdige genotyper (CG og CC) med en høyere frekvens blant CFS-pasientene sammenlignet med referansesettet (p = 0,044). En ikke-signifikant forskjell mellom CFS pasientene og referansesettet ble funnet for β₂ -Adrenerg reseptor SNP ved posisjon Rs 1042713. CFS-pasienter hadde der en høyere frekvens av GG genotype og en lavere frekvens av CG/CC genotypene sammenlignet med referansesettet (p = 0,079).

Innenfor CFS-gruppen var AA (met/met)-genotypen til rs4680 SNP i COMT-genet assosiert med lavere diastolisk blodtrykk (DBP) ved baseline (p = 0,028) og en mindre økning i LF/HF under tilt-testen (p = 0,045) sammenlignet med AG (val/met) og GG (val/val)-variantene (tabell 4). For Rs1042714 SNP β₂- adrenerge reseptorgenet ble ingen statistisk signifikant sammenheng mellom genotyper og kardiovaskulære variabler funnet (tabell 5).
Diskusjonen
Det viktigste funnet i denne studien er den høye frekvensen av AA (met/met) -genotypen av rs4680 SNP i COMT genet blant CFS pasienter.
COMT har en viktig rolle i nedbrytingen av katekolaminer som noradrenalin/norepinefrin og adrenalin/epinefrin (31). A-allelen koder for en substitusjon av aminosyren valin til metionin (Val158Met), og de som er homozygote for denne allelen (Met158met bærere) [low-activity allele ] har en 3- til 4-ganger reduksjon i den nedbrytende enzymatisk aktivitet av katekolaminer sammenlignet med val158val bærere (GG) [high-activity allele] (32, 33).
En nedsatt enzymaktivitet fører til høyere konsentrasjoner av katekolaminer, som kan medføre en forsterkende effekt av sympatisk nerve aktivitet (sympatikus). Dette er helt i tråd med våre tidligere funn av høye nivåer av Noradrenalin/Norepinefrin og adrenalin/epinefrin blant CFS-pasienter, samt en tendens til forsterket sympatisk kardiovaskulær kontroll under ortostatisk stress (2,3,4,5).
Resultatene i denne studien bekrefter også andre resultater fra eksplorative genetiske studier som indikerer en sammenheng mellom CFS og COMT-genet (10). Interessant, lav-aktiv COMT enzym er også utbredt blant pasienter med fibromyalgi, en kronisk smertelidelse, og som har flere kliniske fellestrekk med CFS (12, 13, 14). Således kan AA (met/met)-genotypen av rs4680 SNP i COMT-genet være en genetisk predisponering i både CFS og fibromyalgi.
Gitt de funksjonelle konsekvensene av AA-genotypen (met158met-bærere), var våre funn med lavere baseline DBP og Δ LF/HF (sympatisk respons under tilt) blant homozygote CFS-pasienter overraskende. Disse resultatene er imidlertid i tråd med en nylig rapport fra Hagen og medarbeidere som dokumenterer at GG genotypen (val158val bærere) er assosiert med høyere forekomst av økt systolisk blodtrykk sammenlignet med AA (met/met) og AG (met/val) genotyper (34). En mulig forklaring kan være at redusert nedbrytning av katekolaminer stimulerer sentrale hemmende mekanismer, og forårsaker dermed en demping heller enn stimulering av sympatisk aktivitet.
CFS-pasientene viste en lavere frekvens av GG-genotypen av β₂- adrenerg reseptor SNP rs1042714 (p = 0,044) (tabell 3). G allelen innebærer at glutamin er erstattet av glutamat ved aminosyreposisjon 27 (26). Flere fenotyper har vært assosiert med denne Gln27Glu-polymorfismen, men de funksjonelle effektene forblir uklare (35).
Likevel antyder tidligere undersøkelser at polymorfier av det β₂- adrenerge reseptorgenet er assosiert med tilstander som har flere kliniske trekk som er felles med CFS, for eksempel Temporomandibulær lidelse (preget av kronisk smerte) (15) og Postural ortostatisk Takykardi syndrom (POTS) (11), noe som samsvarer med våre egne resultater.
Den ikke-signifikante forskjell av genotypefrekvenser funnet for den β₂- adrenerge reseptor SNP ved rs1042713 antyder også at denne reseptoren kan spille en rolle i patofysiologien av CFS.
Samlet forslår denne studien at genetisk sårbarhet for CFS kan være relatert til polymorfier av adrenerge kardiovaskulære kontrollgener, noe som støtter hypotesen om endret aktivitet i sympatisk nervesystem som et viktig element i den underliggende patofysiologien (8).
Videre studier bør undersøke detaljer om molekylære mekanismer, så vel som andre elementer av det sympatiske signalisering- og metabolske (katabolisme) systemet, som for eksempel enzymet monoaminoxidase (MAO). Da flere av disse elementene er tilgjengelige for farmakologisk påvirkning, kan slike studier ha direkte klinisk relevans. <– NB!
I NorCapital-studien ble 104 pasienter undersøkt for COMT-genvarians, hvorpå de undersøkte påvirkning og kliniske markører for Klonidin.
Dette var hva de fant:

«Bare mei», Marit @memhj kommenterer:
Her måtte jeg regne ut andelene av genotypene, som står øverst i tabellen. Grunnen til det er at det henger en mystisk uttalelse i fra en av forskerene om at ME-pasientene «trenger» adrenalin??]. Resutalene viser imidlertid at fordeling på COMT genotypene for 104 pasienter var: val/val (19,2%), val/met (49,0%) og met/met (31,7%). Det er eneste val/val homozygoten som har tre til fire ganger økt nedbryting av de andrenerge-stimmulerende-katekolaminene, da i høyst motsetting til HOVEDMAJORITETEN av ME pasientene som har en lav-effektiv nedbrytning, spesielt om du er homozygotisk belemra med å være Met158Met bærer.
I jakten på å finne datamaterialet til Riksens resultater av katekolaminer, ble innsatsen ikke helt bortkasta. I Wyllers phd-publikasjon papir IV og V, kom godsakene frem.
Selv om der er kun 15 pasienter og 63 friske kontroller (HC), er det duket for en praktisk statistikk «se-hvordan-ME-pasienter-egentlig-har-det» oppgave til sammenligning med deres friske klassekamerater.
B
| Katekolaminer i plasma ME vs frisk | ME/CFS Pasient N=15 | Friske kontroller HC N= 53 |
| Adrenalin (pmol/L), gj.snitt | 229 | 171 |
| Adrenalin (pmol/L), 95 % KI | [182-276] | [153-189] |
| Adrenalin (pmol/L), median | 216 | 171 |
| Adrenalin (pmol/L), min-maks | 114-399 | 62-388 |
| Noradrenalin (pmol/L), gj.snitt | 1664 | 1265 |
| Noradrenalin (pmol/L), 95 % KI | [1448-1881] | [1129-1401] |
| Noradrenalin (pmol/L), median | 1646 | 1156 |
| Noradrenalin (pmol/L), min-maks | 926-2621 | 392-1898 |
| Dopamin (pmol/L), median | 157 | 130 |
| Dopamin (pmol/L), 95 % KI | [121-207] | [112-151] |
| Normetanephrine (nmol/L), median | 0,39 | 0,45 |
| Normetanephrine (nmol/L), 95 % KI | [0,21-0,49] | [0,37-0,55] |
| Metanefrin (nmol/L), median | 0,34 | 0,30 |
| Metanefrin (nmol/L), 95 % KI | [0,20-0,41] | [0,27-0,34] |
| 3-Methoxytyramin (3-MT) (nmol/L), median | 0,10 | 0,08 |
| 3-Methoxytyramin (3-MT) (nmol/L), 95 % KI | [0,06-0,13] | [0,07-0,09] |
| Alder, snitt (min-maks), år | 15 (12-18) | 15 (13-18) for N=56 |
| Kjønn ant n= Female, n= Male | F=10, M=5 | M=21 |
| Sykdomsvarighet , snitt (min-maks) | 31(6-60) mnd/2,6 (0,5-5 år) | |
| FSS (mod Fatigueskår) snitt (min-maks) | 4,6 (3,8-5,0) | 1,5 (1,0-3,6) |
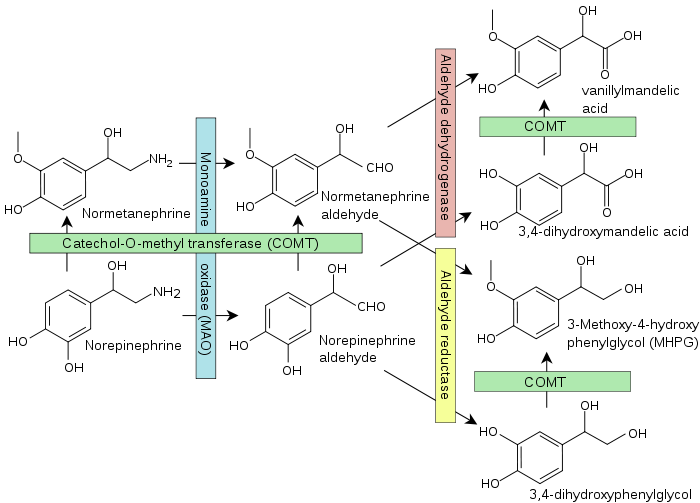
Bildet viser noe av COMT sin oppgave i det metabolske bildet.
Før vi går videre, må vi snakke om Alan Light sin genutrykk-studie av både COMT og hvordan Adrenerge reseptorene påvirker ME pasienter under en liten lett treningsøkt, ja, sånn at det kan bli litt mer forståelig det hele 🙄 :

Her begynner også Karl J. Tronstad og Fluge/Mella sitt team og 200 ME voksne pasienter sin undersøkelse om hvordan aminosyrene oppfører seg i ME, samt Naviaux sin studie (og Hansons (US) og Armstrong (AU) mfl), komme ut i lyset med tanke på dannelse av hemmende stoffer og nedbrytning av intermediater i fra enkelte aminosyrer som er kobla i COMT-systemet (med MAO-enzymer de ikke har undersøkt). Til og med Riksens egen gensutrykk-studie viser økt energikrav i ME-pasientene.
Om vi nå har snakket om adrenerge reseptor proteiner α₂(a), β₁ og β₂ og riksen snakker lite om motstykket til adrenerge stoffer, som acetyl-kolin (iallefall i all glatt musklatur som blodårer og skjelettmuskler, tarm, ikke akkurat lunger som har motsatt effekt-tenk asmamedisin og epi v allergi). og nitrogenmonosyd fra endotele celler og dens nå ikke fullt så gode funksjon lengre. Kolinerge M.ere og litt sånn autantistoffer mot adrenerge reseptorer.
Til jeg elegant hopper over på TRACEAMINER-biogene aminer… intermediater og metabolitter der ikke engang vitenskapen har oppdaget alle sammen ennå (digger peptidfolk-nerdeheroes).

Noen veier til Rome der, reiseveien e brutal….
I blogginnlegget «På ME-fronten: Graverende råd til mennesker med sykdommen Myalgisk Encefalopati (ME)«, er det grunn til å reagere når det anbefales antidepressive og antipsykotiske preperater. I dette tilfellet nevnes «Noen kan også ha nytte av amitriptylin (Sarotex ®)» under behandlingstiltak.
På feks wikipedia kan vi lese mer om virkningsmekanismene til amitriptylin. Medikamenter i samme klasse ersterkt potente på reseptorene som styrer nervessytemet. Sarotex har en relativt sterkt reopptaksmekanisme på noradrenalin, samtitig som den er antikolinerg, og blokker natrium og kalium-reseptorer. Joda, for det står jo i stil med ME-pasienters elendige evne til å bryte ned noradrenalin? Heisan krampeanfall og hallo til fem-gradsnivå av eksploding head-syndrom der alle neuronene gikk amokk samtidig. Trøsten må nu være at den har antihistaminvirkning.
Feks antipsykotiske stoffer som hemmer MAO enzymet. Når slike midler gis, skal det samtidig gis kostholdsveiledning og diett med lite tyramin i. Har du hørt legen gjøre det?
På tynn is, så kan en jo lese denne. om potente midler som utdeles over en lav sko, med lovnad om fantastike frisk-effekt… (helt utrolig…!!!)
På tampen:
Det riksen ikke har gjort så mye av annet enn å registrert symptomer som blir fortalt, som svimmelhet og nærsynkoper osv. For det er vel som lille prinsesse Amy of England og dr. Hyde fra Kanada med årtier med erfaring om du fikk lyst å lære mer. Historen er bare ett par år gammel.
«I started by taking Amy’s blood pressure and heart rate. It was relatively normal at 88 beats-per-minute (bpm) with a blood pressure (bp) of 109/76 mg of mercury. These findings would be considered normal for her age, although 88 bpm might be considered to be a bit rapid for someone lying down in bed.
I asked Amy to stand and her heart rate immediately rose to 116 beats per minute (bpm). Much too fast, but it quickly settled down to 105 bpm, still much too fast for someone doing nothing but standing. At the time, I thought this rapid heart rate might be explained as a result of her lying in bed but, since she had been a little more active recently, I doubt that was the cause. I then proceeded to take Amy’s blood pressure for 10 minutes and this is what I found.»
| Time inminutes | Left ArterialBlood Pressure,
mgm mercury |
Heart ratebpm | Amy is standing 2 inches away from herbed, not talking and trying to stand still. I
am sitting immediately in front of her to catch her should she fall or collapse. |
| In bed | 109/76 | 88 | Lying prone |
| 1 standing | 118/79 | 105 | Standing at attention, not moving or speaking |
| 2 min. | 105/82 | 110 | |
| 3 min. | 118/80 | 118 | |
| 4 min. | 124/81 | 129 | |
| 5 min. | 144/73 | 128 | |
| 6 min. | 124/85 | 133 | |
| 7 min. | 123/81 | 130 | |
| 8 min. | 61/30 | 81 | A precipitous fall in her bloodPressure occurs. Amy loses consciousness and
she falls onto her bed. I lift and massage her legs and she regains consciousness within15 seconds. |
| ? | |||

Noe å tenke på…

